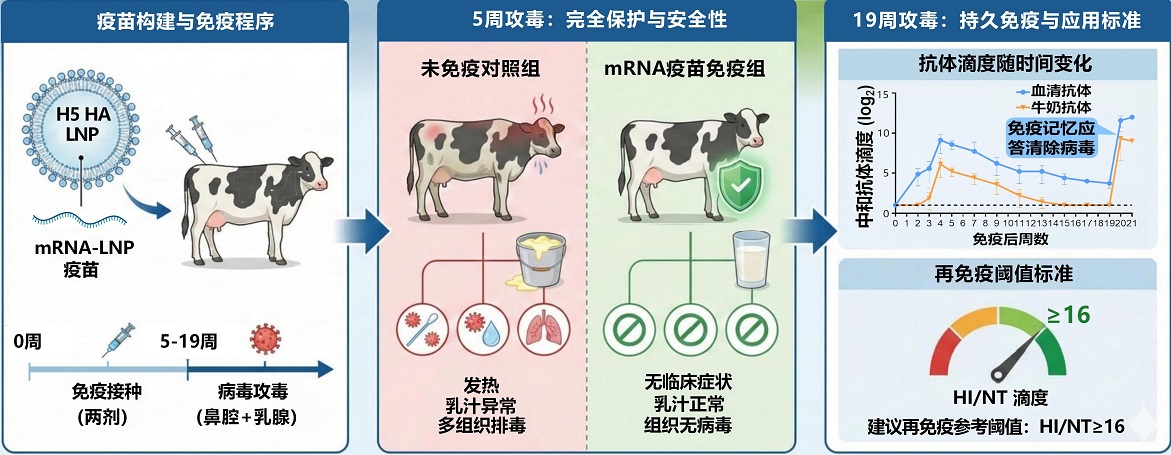
美国在两年时间里,超千座奶牛场遭到H5N1侵袭,荷兰有最新报告显示牛群出现了感染病例,然而全球范围内竟然没有一款可供牛使用的禽流感疫苗。一直到最近,中国农科院哈尔滨兽医研究所陈化兰团队研制出首款H5牛流感mRNA疫苗,该疫苗在泌乳奶牛身上验证了具有100%的保护效力。这不仅仅是技术方面实现了突破,更是给全球的奶牛场预先加装了一道生物安全闸。
mRNA技术首次为奶牛定制
绕开传统疫苗研发慢的困局
传统灭活疫苗,从毒株做筛选,而后到生产上市,常常要耗费数年时间,然而mRNA平台,仅仅只需获取病毒基因序列,便能够快速地进行合成。陈化兰团队,此次所选用的,恰恰正是针对H5亚型流感病毒血凝素蛋白而设计的mRNA-LNP疫苗,从设计开始,一直到完成动物试验,周期被大幅压缩。在2024年的时候,美国奶牛疫情出现暴发情况,倘若当时手中拥有这一技术储备,那么上千牧场的经济损失,原本是可以避免的。
国内首个专攻泌乳奶牛的免疫研究
在此之前,全球范围内,针对奶牛的流感疫苗研究,几乎处于空白状态。大部分的禽流感疫苗,仅仅是在禽类或者小鼠身上进行验证。这个团队,首次选用处于泌乳期的荷斯坦奶牛作为模型,展开系统监测,监测接种之后的产奶量变化,监测乳成分变化,监测临床症状。结果明确显示,所有免疫后的奶牛,采食状况正常,乳房部位没有出现红肿现象,其产奶曲线与未接种疫苗的组相比毫无差异,有力且直接地给出了回答,针对养殖户最为关心的“打了针是否会对下奶产生影响”这一问题。
100%保护力背后有两组关键数据
乳汁中检出高滴度中和抗体
研究团队给奶牛接种了两剂 mRNA 疫苗,之后采集了血清样本和乳汁样本,血凝抑制抗体滴度的均值达到了1:256以上,远远超过了1:40的保护阈值。更为关键的是,乳汁当中还存在着高水平的特异性 IgG 抗体和 IgA 抗体,这表明犊牛通过吮吸初乳能够获得被动免疫,进而形成母幼双屏障。对于依赖鲜奶销售的牧场而言,抗体通过乳汁分泌还能够额外降低生乳带毒的风险。
攻毒试验六头奶牛全部零检出
在免疫之后的第三十五天,团队采用当前的美国流行株H5N1分支针对奶牛实施气管攻毒,对照组的三头奶牛在攻毒之后的第三天,鼻腔拭子的病毒载量便突破了10^4拷贝,乳腺组织之中也检测出了病毒抗原。然而免疫组的六头奶牛连续十四天进行采样都未曾检测出病毒核酸,咽拭子、直肠拭子以及乳汁样本全部呈现阴性,达成了完全保护。这一回的攻毒保护率大幅超过了美国农业部对于禽流感疫苗85%有效性的审批要求。
免疫记忆能撑过整个泌乳期
抗体回落但仍有三成奶牛完全抗毒
可改写为:畜牧业极其担忧疫苗的保护期限没办法撑过一个生产经历时期。该项研究专门进行了时间跨度拉长的观察阶段:在首次免疫往后的19周这段时间,接受免疫的奶牛血清当中的抗体虽从达到高度的数值下降近似直至1:32左右这么个程度,然而再次运用有活性的病毒实施进攻的时候,6头里面有4头依旧能够做到完全的抵御行动,对于病毒的检测结果全部呈现阴性状态。这所表达的意思是在奶牛大约300天时长的泌乳阶段之内,即便抗体出现了减弱的情况,大部分的个体仍然留存着具备免疫记忆功能的保护能力,并不需要每个月都进行补充免疫。
加强针策略已有数据支撑
针对那些抗体落下后丧失保护的少数奶牛,团队设计了二次加强免疫的方案。其结果表明,加强针打完后,抗体滴度在24小时之内迅速地回升,并且峰值水平相较于初免而言更高。这为牧场给予了灵活的操作空间,具体为:在低风险季节能够依赖基础免疫,而在高发期或者跨省调运之前补打一针便能够快速拉起防护网。
人兽共患病防线前移到牛舍
阻断病毒跨物种复制的关键一步
近两年,H5N1 在美国奶牛当中持续传播着,已出现牛传人病例,感染者所具有的结膜炎以及呼吸道症状证实病毒获得了哺乳动物适应性突变。如今疫苗虽不直接应用于人,然而通过消除病毒在牛群里的复制,能够切断从野鸟到家牛再到人的传播链。陈化兰团队采用的 HA 抗原设计跟人类流感疫苗研发路径是同源的,还为后续开发人用牛流感疫苗奠定了基础。
避免重蹈新冠前缺乏动物疫苗的覆辙
疫情初起新冠时,水貂养殖场所出现SARS-CoV-2反向感染人之事件,那时全球毫无可用动物疫苗,只能进行大规模扑杀。此次H5牛流感mRNA疫苗得以诞生,这表明我国在人兽共患病前端控制方面已然提前落子。农业农村部已把牛流感列入优先防控疫病清单,而这款疫苗正是清单之下首个落地的产品。
商业化落地还要闯三关
田间试验需要更多牧场参与
实验室里,6头奶牛得出的数据,尽管看上去十分不错,然而美国那1084个牧场出现的疫情表明,病毒能够借助挤奶设备,通过运输车辆,依靠人员鞋底迅速传播。接下来,一定要于开放式牧场展开千头级规模的田间试验,以此去验证疫苗在不同饲养密度情形下,于不同挤奶频率情况下,在混合感染压力状况下的实际效果。当下,团队已经跟黑龙江、内蒙古两家万头牧场进行了接洽,预计在今年三季度启动试点。
注册审批通道尚待明确
当下国内并没有专门针对牛使用的mRNA疫苗的评审指导原则,至于按照化药、生物制品或者创新兽药来进行申报,目前尚无先例。参照美国农业部针对梅里亚公司禽流感疫苗的紧急使用授权路径,该研究团队正跟中国兽医药品监察所展开沟通,力争参照高致病性禽流感疫苗的应急评价程序,把审评周期从常规的3年压缩至12个月以内。
国际竞争已到赛点
美国着急但技术路线卡壳
美国国家动物疫苗中心于2024年便立项去研发奶牛H5N1疫苗,选择的病毒样颗粒这个途径在奶牛身上免疫原性不好,两次攻毒保护率大概只有60%,并且没办法在乳汁里检测出抗体。今年2月美国农业部紧急进行mRNA流感兽用疫苗招标,当前只有三家初创企业响应,最快要到2027年才可以进入临床试验。这表明未来两年我国或许会成为全球唯一能够提供牛流感疫苗的国家。
世卫组织已将牛株纳入候选疫苗库
近来,因奶牛疫情已蔓延至欧洲,世界卫生组织把美国分离株B3.13以及欧洲分离株D.1.1同时纳入人用大流行候选疫苗毒株名单。陈化兰团队所研发的疫苗正好是基于HA保守表位,对那两种流行株都具备交叉中和作用。一旦世界卫生组织开启大流行应对程序,此疫苗技术能够迅速转产人用版本,给全球流感防控拿出中国方案。
身为奶牛养殖场负责人,面对周边国家牛群感染情况陆续出现,你是会主动采购处于试验阶段的新疫苗给健康牛群接种呢,还是等疫情逼近门口才去谋划应对呢?欢迎在评论区分享你的风险管理经验,也请将文章转给身边的畜牧从业人士,让更多人知晓我们手头已然有可用武器了。